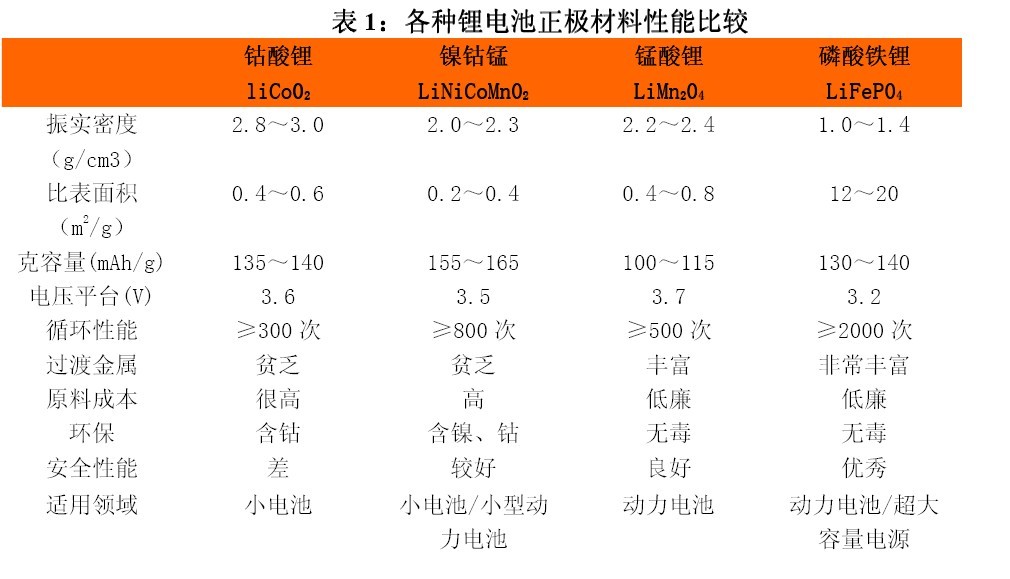
鋰離子電池現使用的正極材料有如下幾種:
1、鈷酸鋰
鈷酸鋰也是目前應用最為廣泛的正極材料,鈷產生3.9V(vs. Li)的電勢平臺,對鈷酸鋰而言,對應于其理論容量,高達274mAh/g,實際容量可達155mAh/g具有很高的能量密度。主要應用于便攜電池領域:如手機,PDA;移動DVD;MP3/MP4、筆記本電腦。
1)結構缺陷
對鈷酸鋰(LixCoO2,0<x<1)而言,當x=1 時,對應于其理論容量,高達274mAh/g,但在實際的循環過程中,當x>0.55 時,材料的容量發生嚴重的退化,其層狀結構傾向于塌陷,使得實際可利用的容量不超過155mAh/g,為了能夠更多的利用LiCoO2 中的鋰離子,人們采用摻雜、包覆等辦法對其改性。目前,有多種元素應用于LiCoO2 摻雜,但只有Mn 和Al 表現出較好的效果。在Li 過分脫出時(E>4.2V 時),LiCoO2 發生嚴重的過充現象,化學鍵發生斷裂而釋出O2,導致體系的不穩定,甚至有使電池爆炸的危險。
2)資源缺乏
鈷在我國屬于稀缺資源,我國鈷礦礦床規模較小,礦區儲量大于2 萬噸的只有甘肅金川和青海德爾尼兩處,礦區儲量大于1 萬噸的有河北、四川、海南、新疆4 省。截至2006 年底,我國探明鈷儲量47.1 萬噸。由于連年開采,我國鈷儲量逐年減少。我國鈷產量應該在4900 噸左右。2002 年我國鈷消費量為4845 噸,比2001 年增加了22%。從2002 年起,電池行業已超過硬質合金行業,成為我國鈷消費的第一大行業。由于目前我國未發現大規模有開采價值的鈷礦,我國鋰電池正極材料用鈷酸鋰的生產基本上是從國外進口價格昂貴鈷原料。
2、鎳酸鋰
Ni4+/Ni3+電對能產生3.75V 的電勢平臺。它能可逆的嵌脫0.7Li,具有接近200mAh/g 的循環容量,但在實際中,很難得到這個結果。首先在高溫下,由于Li 的揮發,很難合成化學計量比LiNiO2,高溫時六方相的LiNiO2 很容易向立方相的LiNiO2 轉變,這種鋰鎳置換的立方相的沒有電化學活性,而且這個反應的逆過程很慢并且不完全。此外在充放電過程中,LiNiO2 還會發生一系列的結構變化,而導致嵌鋰容量的損失。實際上鎳酸鋰無太大實用價值。
3、鎳鈷二元材料和多元復合材料
LiCoO2 價格昂貴,LiNiO2 合成困難,如果能夠結合二者的優點,用價格相對低廉的Ni 替代部分Co,合成具有LiCoO2 一樣優良電化學性能地電極材料,那么將具有廣闊的應用前景。由于半徑相近,Ni 和Co 幾乎可以以任何比例形成固溶體。近幾年來,多元混合摻雜的層狀氧化物得到了大量的研究,不同金屬原子比例的鎳鈷錳多元材料得到了研究,但是顆粒形貌和粒度分布不得到有效的控制,只有在足夠高的電勢下(大于4.5V)才能獲得180mAh/g 的容量,此外沒有從根本上改變鈷系材料的特點。
4、尖晶石錳酸鋰
尖晶石錳酸鋰能夠產生4.0 V 的電壓平臺,與鈷酸鋰相當,理論容量148mAh/g,實際容量120mAh/g 左右,比現在所用的鈷酸鋰稍低。早在上世紀80年代Goodenough 就發現鋰離子能夠在尖晶石結構的錳酸鋰中電化學可逆的嵌脫,從而得到了眾多研究者的關注。與鈷酸鋰和鎳酸鋰相比,錳酸鋰原料來源廣泛,價格非常便宜(只有Co 的10%),而且沒有毒性,對環境友好。曾一度被認為是替代LiCoO2 的首選鋰離子電池正極材料。尖晶石LiMn2O4 的容量衰減主要來源于:一方面為強烈的電子-晶格作用,即Jahn-Teller 效應,在放電過程中,尖晶石顆粒表面會形成Li2Mn2O4 或形成Mn 的平均化合價低于3.5 的缺陷尖晶石相,這會引起結構不穩定,造成容量的損失。另一個方面在于循環過程中Mn 的溶解流失,由Mn3+很容易發生歧化反應,生成Mn2+和Mn4+;Mn2+溶解于電解液中而造成Mn 的流失。所以一直以來市場受到嚴重限制。
5、橄欖石型磷酸鐵鋰
研究人員發現在三維框架結構中,引入含氧多的陰離子如(SO4)2-或(PO4)3-等來取代O2-,除了得到與氧化物一致的高電壓外,也能提供較大的自由體積,有利于鋰離子的遷移,而且使鋰的嵌入和脫嵌電位保持穩定。1997 年,Goodenough 等首次報道了橄欖石型的磷酸鐵鋰(LiFePO4)可用于鋰離子電池正極材料,其中的鋰離子可以完全從晶格中脫出形成層狀FePO4,其相對于鋰的電極電勢為3.5 伏,理論容量為170mAh/g。